Od dawna istnieją obawy, że kobiety z HIV, które przyjmują pewne leki przeciwretrowirusowe w czasie ciąży, mogą być narażone na zwiększone ryzyko wad wrodzonych. Badania są często sprzeczne, a obawy dotyczące potencjalnych zagrożeń mogą czasami wypaczyć nasze wyobrażenie o faktycznym bezpieczeństwie leku.
Morsa Images / Getty Imagestło
Lek przeciwretrowirusowy Sustiva (efawirenz) od dawna budzi obawy, a wcześniejsze wytyczne dotyczące leczenia odradzały jego stosowanie, przynajmniej w pierwszym trymestrze ciąży, ze względu na możliwe ryzyko działania teratogennego (wady wrodzone).
Od tego czasu zalecenia uległy zmianie i obecnie zezwalają na stosowanie preparatu Sustiva, aczkolwiek jako alternatywa dla preferowanych środków, takich jak Descovy (emtrycytabina + tenofowir AF), Prezista (darunawir) i Isentress (raltegrawir).
Te same alarmy zabrzmiały w 2018 i 2019 roku w sprawie Tivicay (dolutegrawiru), leku przeciwretrowirusowego, który, jak się uważa, był powiązany z 11 przypadkami wad cewy nerwowej w Rwandzie i Botswanie.
W odpowiedzi na te wczesne doniesienia Departament Zdrowia i Opieki Społecznej Stanów Zjednoczonych (DHHS) przeniósł Tivicay do „alternatywnego statusu”, co od tego czasu zostało uchylone. W lutym 2021 roku, po szeroko zakrojonym dochodzeniu, Tivicay po raz kolejny otrzymało „preferowany status” dla osób próbujących zajść w ciążę.
Te ostrzeżenia wprawiły wiele osób w zakłopotanie, czy te antyretrowirusy stanowią realne zagrożenie dla nienarodzonego dziecka, a jeśli tak, to ile?
Sustiva
Oceniając rzeczywiste ryzyko wad wrodzonych związanych z lekami przeciwretrowirusowymi, większość aktualnych dowodów pochodzi z badań na zwierzętach i zapisów dotyczących ciąż antyretrowirusowych.
W większości przypadków badania na zwierzętach były odpowiedzialne za uruchamianie alarmów, co skłoniło DHHS i inne osoby do podjęcia proaktywnych środków w celu zbadania roszczeń (czasami w ciągu lat) i do tego czasu „zahamowanie” leku.
Tak było w przypadku Sustivy.
Badania na zwierzętach
Obawy dotyczące teratogenności wywołanej przez Sustivę pojawiły się po raz pierwszy w 1998 r., Kiedy trzy z 20 małp cynomolgus narażonych na działanie leku urodziły dzieci z rozszczepami podniebienia i wadami cewy nerwowej. Niepokojący był fakt, że względne stężenie leku było tylko 1,3 razy wyższe niż stosowane u ludzi.
Inne badania wykazały, że szczury narażone na działanie preparatu Sustiva doświadczyły resorpcji płodu, zjawiska, w którym płody, które zmarły podczas ciąży, były ponownie wchłaniane przez pozostałe rodzeństwo.
Pomimo ważności tych badań, wyniki ogólnie nie były spójne, a niektóre badania nie wykazały związku między Sustivą a wadami wrodzonymi u myszy i królików.
Badania epidemiologiczne
Choć odkrycia były uderzające, to samo zaobserwowano u ludzi. Chociaż we wczesnym przeglądzie Antyretrowirusowego Rejestru Ciąż (APR) zidentyfikowano wady wrodzone u 27 z 1142 dzieci narażonych na działanie preparatu Sustiva w pierwszym trymestrze ciąży, niska częstość występowania wad cewy nerwowej - dominujące typy obserwuje się w badaniach na zwierzętach - budzi wątpliwości, czy lek faktycznie stanowił zagrożenie dla ludzkich płodów.
Według danych APR od 1989 do 2020 roku, odsetek wad wrodzonych u dzieci narażonych na działanie preparatu Sustiva w czasie ciąży nie różni się od odsetka dzieci w ogólnej populacji USA.
Późniejsza analiza w krajach o niskich i średnich dochodach dała podobne wyniki, w których odnotowano 44 wady wrodzone wśród 2026 dzieci narażonych na działanie preparatu Sustiva w czasie ciąży.
Podobne badania przeprowadzone we Francji potwierdziły wyniki jedynie w przypadku 372 wad wrodzonych z 13 124 żywych urodzeń, z których żaden nie dotyczył wad cewy nerwowej obserwowanych u zwierząt.
Mimo to amerykańska Agencja ds.Żywności i Leków (FDA) nadal zaleca kobietom unikanie ciąży podczas przyjmowania preparatu Sustiva oraz doradza swoim lekarzom, aby unikali tego leku w pierwszym trymestrze ciąży.
Tivicay
W przeciwieństwie do Sustivy, większość obaw związanych z Tivicay i ryzykiem wad wrodzonych wywołały pojedyncze doniesienia o teratogenności w Afryce.
W Botswanie zabrzmiały dzwonki alarmowe, gdy badanie z 2019 roku finansowane przez National Institutes ujawniło, że odsetek wad cewy nerwowej był wyższy wśród kobiet przyjmujących Tivicay w porównaniu z jakimkolwiek innym lekiem przeciwretrowirusowym (0,3% do 0,1%).
Jednak gdy zakres badania został rozszerzony, ten sam zespół naukowców odkrył, że 0,19% dzieci narażonych na Tivicay w czasie ciąży miało wady cewy nerwowej w porównaniu z 0,2% w przypadku wszystkich innych leków przeciwretrowirusowych - różnica nieistotna statystycznie.
Przypuszczano, że głównym czynnikiem powodującym występowanie wad cewy nerwowej w tej populacji afrykańskich dzieci nie były leki przeciwretrowirusowe, ale powszechny niedobór kwasu foliowego.
W Stanach Zjednoczonych i innych krajach rozwiniętych suplementacja kwasu foliowego jest zalecana w celu zmniejszenia ryzyka wad cewy nerwowej, takich jak rozszczep kręgosłupa i bezmózgowie. Tego samego brakuje w krajach afrykańskich, takich jak Botswana.
Na podstawie zaktualizowanych danych z APR (w których odsetek wad wrodzonych spowodowanych prenatalną ekspozycją na Tivicay nie różnił się od ogólnej populacji), DHHS przywrócił Tivicay jako preferowany środek w czasie ciąży wraz z pięcioma innymi lekami.
Inne leki przeciwretrowirusowe
W 2014 roku naukowcy z francuskiej kohorty okołoporodowej opublikowali badanie, w którym zbadano liczbę wad wrodzonych obserwowanych u dzieci narażonych na różne leki przeciwretrowirusowe w czasie ciąży. W międzynarodowym badaniu wzięło udział łącznie 13124 dzieci urodzonych przez kobiety zakażone wirusem HIV od 1986 roku.
Chociaż wzrost wad wrodzonych był związany z niektórymi lekami przeciwretrowirusowymi, takimi jak Crixivan (indynawir) - lek, który nie jest już używany w Stanach Zjednoczonych - wskaźnik nadal nie różnił się od wskaźnika w populacji ogólnej. Co więcej, nie znaleziono żadnego konkretnego wzoru w rodzaju lub ciężkości wad wrodzonych.
Nie oznacza to, że leki nie niosą ze sobą żadnego ryzyka. Francuscy naukowcy odnotowali dwukrotny wzrost wad serca u niemowląt narażonych na działanie zydowudyny (AZT). Większość z nich dotyczyła ubytku przegrody międzykomorowej, powszechnej wady wrodzonej, w której między dwiema dolnymi komorami serca powstaje dziura.
Badania przeprowadzone przez Harvard School of Public Health opublikowane w 2014 roku potwierdziły wiele francuskich ustaleń. Jednak wśród 2580 dzieci narażonych na leki przeciwretrowirusowe w pierwszym trymestrze ciąży żadna klasa leków nie wiązała się ze zwiększonym ryzykiem wad wrodzonych w porównaniu z tym, co obserwowano u ogółu społeczeństwa.
Naukowcy z Harvardu zauważyli zwiększone ryzyko chorób skóry i układu mięśniowo-szkieletowego u dzieci narażonych na działanie Reyatazu wzmocnionego rytonawirem (atazanawir) w pierwszym trymestrze ciąży. Chociaż zalecono dalsze badania, naukowcy nadal doszli do wniosku, że ogólne ryzyko jest niskie.
Słowo od Verywell
Jeśli jesteś w ciąży lub planujesz zajść w ciążę, ważne jest, aby porozmawiać z lekarzem o korzyściach i ryzyku stosowania jakiegokolwiek leku przeciwretrowirusowego, aby dokonać świadomego wyboru.
Jest to szczególnie ważne, ponieważ od 2018 roku zarejestrowano mnóstwo nowych leków, w tym Biktarvy (biktegrawir + emtrycytabina + tenofowir AF), Cabenuva (kabotegrawir + rylpiwiryna do wstrzykiwań), Pifeltro (dorawiryna), Rukobia (fostemsawir) i Trogabarzo (ibalizsawir). -uiyk). Brak wystarczających danych do oceny bezpieczeństwa tych leków w czasie ciąży.
Ważne jest, aby pamiętać, że karmienie piersią jestniezalecane dla każdej matki zakażonej wirusem HIV, niezależnie od leku przeciwretrowirusowego. Biorąc pod uwagę dostępność odżywczych preparatów dla niemowląt, władze Stanów Zjednoczonych zalecają karmienie piersią w celu dalszego zmniejszenia ryzyka przeniesienia wirusa HIV z matki na dzieci.
Co się stanie, jeśli Twoje dziecko ma HIV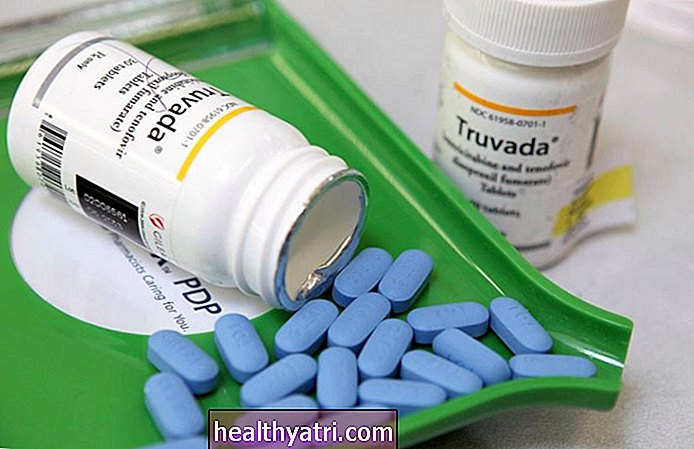
.jpg)












.jpg)





-for-kids-with-autism.jpg)



