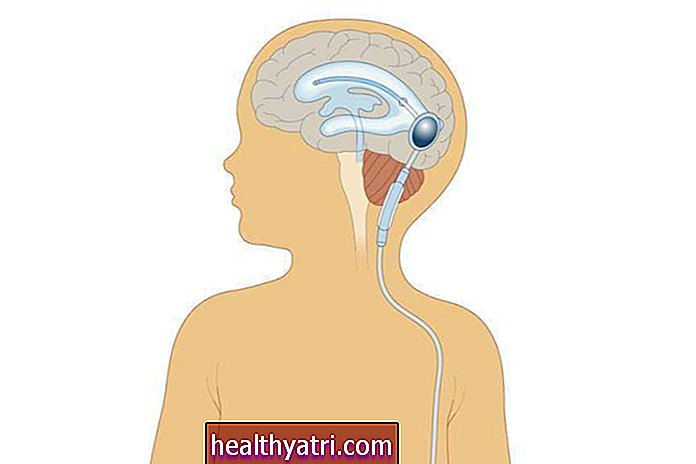
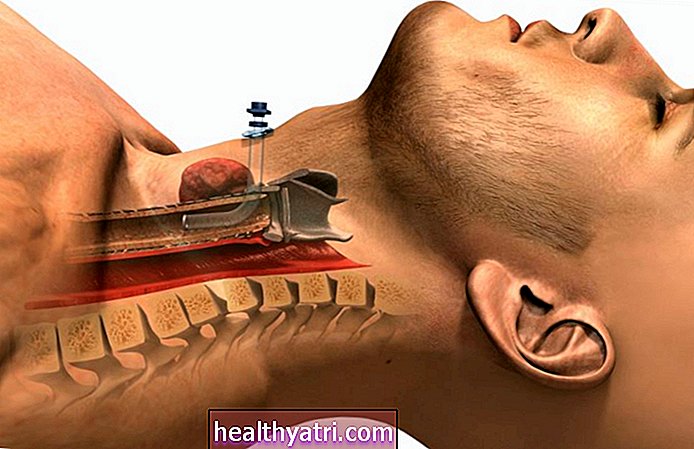
Zespół Li-Fraumeni lub LFS to choroba genetyczna, która predysponuje ludzi do wielu różnych nowotworów. Osoby z LFS często rozwijają te nowotwory wcześniej w życiu, niż jest to typowe dla populacji ogólnej. W LFS może również występować większe ryzyko drugiego lub kolejnych nowotworów.
Zespół został po raz pierwszy rozpoznany w kilku rodzinach, u których we wczesnym okresie życia rozwinęło się wiele różnych rodzajów raka, zwłaszcza mięsaków. Ponadto wydaje się, że członkowie rodziny są bardziej narażeni na rozwój wielu nowych i różnych nowotworów w ciągu życia. Frederick Li i Joseph Fraumeni Jr, byli lekarzami, którzy po raz pierwszy zgłosili te odkrycia w 1969 roku i tak LFS otrzymało swoją nazwę.
Hero Images / Getty ImagesDlaczego wyższe ryzyko raka?
Osoby z zespołem Li-Fraumeni są bardziej narażone na raka, ponieważ odziedziczyły tak zwaną mutację linii zarodkowej w ważnym genie zwanymTP53.
Mutacja linii zarodkowej to zmiana genetyczna, która nastąpiła w linii zarodkowej rodziców osoby dotkniętej chorobą - to znaczy mutacja początkowo występuje w komórkach jajników lub jąder, które dają początek komórkom jajowym i plemnikom. Mutacje w tych komórkach to jedyne rodzaje mutacji, które mogą zostać przekazane bezpośrednio potomstwu w momencie poczęcia, kiedy jajo i nasienie spotykają się, tworząc zygotę. Zatem mutacje linii zarodkowej wpłyną na każdą komórkę ciała nowego potomstwa; przeciwnie, mutacje somatyczne rozwijają się gdzieś u osobnika w pewnym momenciepopoczęciem lub dużo, dużo później, i wpływają na zmienną liczbę komórek w ciele.
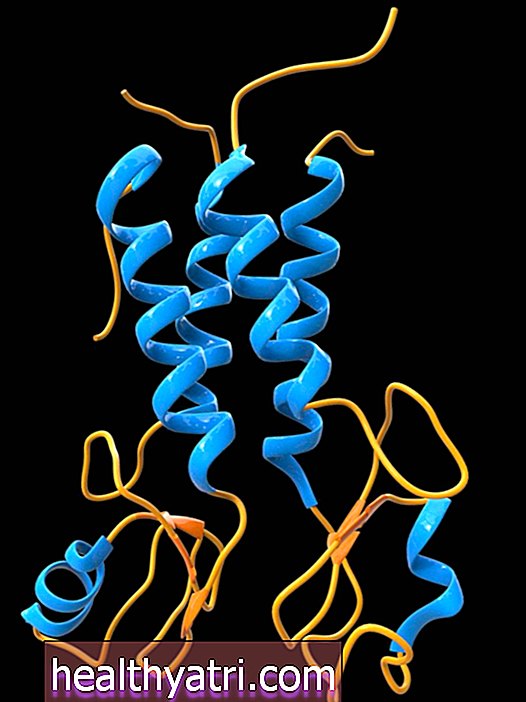
Kluczowe mutacje linii germinalnej w rodzinach z LFS to te, które wpływają na funkcjęTP53gen. W świecie badań nad rakiemTP53 gen jest tak ważny, że nazwano go „strażnikiem genomu”.
TP53 jest genem supresorowym guza - to znaczy jest genem, który chroni komórkę przed jednym krokiem na drodze do raka. Kiedy ten gen ulega mutacji w taki sposób, że nie działa zgodnie z przeznaczeniem lub w wyniku znacznego ograniczenia jego funkcji, komórka może rozwinąć się w raka, często w połączeniu z innymi zmianami genetycznymi. Testowanie dlaTP53 Mutacje linii germinalnej zostały po raz pierwszy opracowane w 1990 roku, kiedy potwierdzono związek między p53 i LFS. Od tego czasu prawie 250 mutacji w całymTP53 gen został wykryty.
Mutacja w innym genie, hCHK2, również została powiązana z LFS; jednak jego znaczenie jest niejasne. Gen hCHK2 jest genem supresorowym nowotworu, który jest aktywowany w odpowiedzi na uszkodzenie DNA. Tylko niewielka liczba rodzin jest nosicielami tej mutacji, a osoby dotknięte chorobą mają podobny zakres nowotworów, jak te z mutacjami TP53.
Jak wysokie jest ryzyko?
Szacuje się, że ogólnie osoba z LFS ma 50% szans na raka w wieku 40 lat i aż 90% w wieku 60 lat. Jeśli masz LFS, Twoje indywidualne ryzyko częściowo zależy. czy jesteś mężczyzną czy kobietą, przy czym kobiety są generalnie bardziej narażone na ryzyko niż mężczyźni.
Jeśli spojrzymy na ryzyko zachorowania na raka w ciągu całego życia u mężczyzn i kobiet z LFS w wieku 50 lat, ryzyko zachorowania na raka przedstawia się następująco: 93% dla kobiet i 68% dla mężczyzn. Jeśli zachoruje na raka, kobiety mają również tendencję do rozwoju tego nowotworu w młodszym wieku: średnio 29 lat, w porównaniu do 40 lat u mężczyzn.
Według badań Mai i współpracowników większe ryzyko u kobiet wynika głównie z wczesnego raka piersi. Badacze ci odkryli również, że wśród kobiet, które uzyskały wynik pozytywnyTP53mutacje, rak piersi był zdecydowanie najczęstszym nowotworem złośliwym. Skumulowana zachorowalność na raka piersi wynosiła około 85% w wieku 60 lat. W tym samym badaniu ryzyko raka piersi znacznie wzrosło u kobiet w wieku 20 lat, co potwierdza, że badania przesiewowe w kierunku raka piersi rozpoczynające się w wieku 20 lat są dobrą praktyką u kobiet z LFS.
Ten poziom ryzyka dlaTP53mutacje są porównywalne do tych obserwowanych u kobiet z mutacjami linii zarodkowych w genach BRCA1 i BRCA2 - genach, które zyskały na znaczeniu, gdy media donosiły o testach genetycznych mutacji BRCA1 / 2 i prewencyjnych mastektomiach (przez celebrytów, takich jak Angelina Jolie).
Jakie są główne rodzaje raka?
Każdy nowotwór może rozwinąć się u każdego człowieka w dowolnym momencie. Wiadomo jednak, że osoby z LFS mają wczesne diagnozy raka i wysokie ryzyko życiowe kilku „podstawowych” rodzajów raka, w tym:
- Osteosarcoma - najczęstszy rodzaj raka, który zaczyna się w kościach
- Mięsaki tkanek miękkich - rodzaj raka, który rozwija się z pewnych tkanek, takich jak tłuszcz, mięśnie, nerwy, tkanki włókniste, naczynia krwionośne lub tkanki głębokiej skóry
- Rak piersi o wczesnym początku
- Nowotwór mózgu
- Białaczka - rak komórek krwiotwórczych
- Rak kory nadnerczy - rak kory nadnerczy, która jest zewnętrzną warstwą nadnerczy (nadnercza leżą nad nerkami i odgrywają ważną rolę w różnych funkcjach hormonalnych)
W badaniu Kleihuesa z 1997 r. Najczęściej identyfikowanym mięsakiem w LFS był kostniakomięsak, odpowiadający 12,6% przypadków, następnie guzy mózgu (12%) i mięsaki tkanek miękkich (11,6%). Spośród mięsaków tkanek miękkich najczęściej identyfikowano mięsaki prążkowanokomórkowe. Inne, rzadziej zgłaszane mięsaki obejmują włókniakomięsaki (które nie są już uważane za prawdziwą jednostkę), atypowe włókniakomięsaki, mięśniakomięsaki gładkokomórkowe, tłuszczakomięsaki oczodołu, mięsaki wrzecionowokomórkowe i niezróżnicowane mięsaki wielopostaciowe. Nowotwory hematologiczne lub raki krwi (takie jak ostra białaczka limfoblastyczna i chłoniak Hodgkina) oraz raki kory nadnerczy występowały z częstością odpowiednio 4,2% i 3,6%.
Ponieważ zidentyfikowano więcej rodzin z mutacjami genetycznymi typowymi dla LFS, implikowano o wiele więcej nowotworów.
Spektrum raka LFS rozszerzyło się o czerniaka, raka płuc, przewodu pokarmowego, tarczycy, jajnika i inne.
Na podstawie tradycyjnych ocen, ryzyko rozwoju mięsaka tkanek miękkich i raka mózgu wydaje się być największe w dzieciństwie, podczas gdy ryzyko kostniakomięsaka może być najwyższe w okresie dojrzewania, a ryzyko raka piersi u kobiet znacznie wzrasta w wieku około 20 lat i utrzymuje się w starszym wieku wiek dojrzały. Statystyki te mogą jednak ulec zmianie, ponieważ praktyki testowania genów predyspozycji do raka ewoluowały.
Jak definiuje się zespół Li-Fraumeni?
Istnieją różne kryteria i definicje tego zespołu. Niektórzy są bardziej inkluzywni niż inni. Klasyczna LFS jest najbardziej restrykcyjną definicją, ponieważ wymaga rozpoznania mięsaka przed 45 rokiem życia, podczas gdy kolejne definicje, takie jak kryteria Chompreta, próbują zawęzić ewolucję wiedzy naukowej na temat typów i wieku guza w momencie rozpoznania.
Klasyczne kryteria LFS:
- Zdiagnozowano mięsaka (rodzaj raka, który obejmuje komórki pochodzenia mięśniowego / szkieletowego / stawów / tłuszczu) przed 45 rokiem życia i
- Mieć krewnego pierwszego stopnia (rodzica, rodzeństwo lub dziecko) z jakimkolwiek rakiem zdiagnozowanym przed 45 rokiem życia i
- Miej innego krewnego pierwszego lub drugiego stopnia (w tym ciotki, wujków i nie tylko) z jakimkolwiek rakiem zdiagnozowanym przed 45 rokiem życia lub mięsakiem zdiagnozowanym w dowolnym wieku.
Kryteria typu Li-Fraumeni (LFL):
- Kryteria LFL tworzą szerszą siatkę obejmującą inne typy raka i niektórych krewnych zdiagnozowanych po 45 roku życia, a stosowane są dwie różne definicje:
- Definicja brzozy: zdiagnozowano u Ciebie jakikolwiek nowotwór dziecięcy lub mięsak, guz mózgu lub rak kory nadnerczy zdiagnozowany przed 45 rokiem życia i masz u krewnego pierwszego lub drugiego stopnia typowego raka Li-Fraumeni (mięsak, rak piersi, guz mózgu, raka kory nadnerczy lub białaczkę) w każdym wieku i u krewnych pierwszego lub drugiego stopnia z jakimkolwiek rakiem przed ukończeniem 60. roku życia.
- Definicja węgorza: Masz dwóch krewnych pierwszego lub drugiego stopnia z nowotworami związanymi z Li-Fraumeni (mięsakiem, rakiem piersi, guzem mózgu, białaczką, guzem kory nadnerczy, czerniakiem, rakiem prostaty, rakiem trzustki) w każdym wieku.
Kryteria Chompret:
- Masz guz należący do spektrum guzów Li-Fraumeni (mięsak tkanek miękkich, kostniakomięsak, przedmenopauzalny rak piersi, guz mózgu, rak kory nadnerczy, białaczka lub rak oskrzelowo-pęcherzykowy płuc) przed 46 rokiem życia i masz co najmniej jedną pierwszą lub drugą -stopni krewniacy z guzem Li-Fraumeni (z wyjątkiem raka piersi, jeśli masz raka piersi) przed 56 rokiem życia lub z wieloma guzami lub
- Masz wiele guzów (z wyjątkiem wielu guzów piersi), z których dwa należą do spektrum guzów Li-Fraumeni, a pierwszy wystąpił przed 46 rokiem życia lub
- Niezależnie od historii rodzinnej, zdiagnozowano raka kory nadnerczy lub guz splotu naczyniówkowego.
Według przeglądu LFS przeprowadzonego przez Schneider i współpracowników, co najmniej 70% osób zdiagnozowanych klinicznie (to znaczy przy użyciu definicji takich jak te powyżej) ma możliwą do zidentyfikowania szkodliwą mutację linii zarodkowej wTP53gen supresorowy guza.
Zarządzanie nowotworami
Jeśli osoba z LFS zachoruje na raka, zaleca się rutynowe leczenie raka, z wyjątkiem raka piersi, w którym zamiast lumpektomii zaleca się mastektomię, aby zmniejszyć ryzyko drugiego raka piersi i uniknąć radioterapii.
Osobom z LFS zaleca się unikanie radioterapii, gdy tylko jest to możliwe, aby ograniczyć ryzyko wtórnych nowotworów złośliwych wywołanych promieniowaniem. Jeśli jednak radioterapia zostanie uznana za medycznie niezbędną do zwiększenia szans przeżycia z powodu danego nowotworu, może być zastosowana według uznania lekarza prowadzącego i pacjenta.
Kontrola i nadzór
Eksperci są coraz częściej proszeni o wypracowanie konsensusu co do tego, jak należy badać rodziny z FLS i jak się nimi opiekować. Niestety, chociaż nauka szybko się rozwija, nie ma jeszcze takiego konsensusu we wszystkich dziedzinach.
Częstotliwość szkodliwychTP53 mutacje w populacji ogólnej są nieznane, a prawdziwa częstość występowania FLS nie jest znana. Szacunki wahają się od 1 na 5000 do 1 na 20000. Im więcej rodzin przechodziTP53testów, rzeczywiste rozpowszechnienie LFS może stać się jaśniejsze.
Zajmowanie się ryzykiem raka piersi
W Stanach Zjednoczonych wytyczne National Comprehensive Cancer Network (NCCN) zalecają coroczne MRI piersi u osób z FLS w wieku od 20 do 29 lat oraz coroczne MRI i mammografię od 30 do 75 lat. W Australii krajowe wytyczne zalecają wykonanie obustronnej mastektomii; w przeciwnym razie zaleca się coroczne MRI piersi od 20 do 50 lat. Schon i współpracownicy zalecają rozważenie opcji zmniejszenia ryzyka obustronnej mastektomii lub badań przesiewowych piersi u kobiet bez raka z mutacją wTP53 gen.
Zalecenia NCCN
Opierając się na odkryciu, że ryzyko raka piersi znacznie wzrasta po drugiej dekadzie, zalecenia obejmowały rozważenie obustronnej mastektomii od 20 roku życia. Roczny szczyt ryzyka raka piersi osiąga około 40-45 lat, a następnie spada, tak że obustronna mastektomia jest rzadziej przynosić korzyści kobietom powyżej 60 lat.
- Świadomość piersi od 18 roku życia z okresowym, konsekwentnym samobadaniem piersi.
- Kliniczne badanie piersi, co 6–12 miesięcy, począwszy od wieku 20 lat
- Wiek 20–29 lat, coroczne badanie MRI piersi z kontrastem
- Wiek 30–75 lat, coroczne badanie MRI piersi z kontrastem i mammografią z uwzględnieniem tomosyntezy
- Wiek> 75 lat, leczenie należy rozpatrywać indywidualnie.
- Dla kobiet zTP53mutacji, u których leczono raka piersi i które nie przeszły obustronnej mastektomii, należy kontynuować badanie przesiewowe z corocznym rezonansem magnetycznym piersi i mammografią, jak opisano powyżej.
- Kiedy omawia się opcję mastektomii zmniejszającej ryzyko, należy zasięgnąć porady dotyczącej stopnia ochrony, stopnia ryzyka raka związanego z wiekiem, opcji rekonstrukcji i konkurencyjnego ryzyka innych nowotworów. W takich dyskusjach należy uwzględnić psychospołeczne, społeczne i związane z jakością życia aspekty poddania się mastektomii zmniejszającej ryzyko.
Zajmowanie się innymi zagrożeniami związanymi z rakiem
Zalecenia NCCN
- Kompleksowe badanie fizykalne, w tym badanie neurologiczne z wysokim wskaźnikiem podejrzenia rzadkich nowotworów i wtórnych nowotworów złośliwych u osób, które przeżyły raka, co 6–12 miesięcy.
- Kolonoskopia i górna endoskopia co 2–5 lat, począwszy od wieku 25 lat lub 5 lat przed najwcześniejszym rozpoznanym rakiem okrężnicy w rodzinie (w zależności od tego, co nastąpi wcześniej).
- Coroczne badanie dermatologiczne rozpoczynające się w wieku 18 lat.
- Coroczny rezonans magnetyczny całego ciała
- Coroczny rezonans magnetyczny mózgu może być wykonywany jako część rezonansu magnetycznego całego ciała lub jako oddzielne badanie.
Inne formy kontroli i nadzoru
Przeprowadzono pilotażową próbę pozytonowej tomografii emisyjnej (FDG-PET) / tomografii komputerowej u dorosłych z LFS, w której wykryto guzy u trzech z 15 osób. Te skany PET-CT, chociaż świetnie nadają się do wykrywania niektórych guzów, również zwiększają ekspozycję na promieniowanie za każdym razem, gdy są wykonywane, więc ta metoda skanowania została zatrzymana i została przeniesiona na MRI całego ciała u dorosłych zTP53szkodliwe warianty.
Kilka grup badawczych zaczęło stosować intensywny program badań przesiewowych, który obejmuje szybki rezonans magnetyczny całego ciała, rezonans magnetyczny mózgu, badanie ultrasonograficzne jamy brzusznej i testy laboratoryjne czynności kory nadnerczy. Ten rodzaj programu nadzoru może poprawić przeżycie osób z LFS poprzez wykrywanie guzów, zanim pojawią się jakiekolwiek objawy, ale potrzeba więcej badań, aby wykazać, że ten rodzaj schematu działa u dorosłych i dzieci z LFS.
Osoby z LFS zostały zapytane o ich stosunek do nadzoru nad rakiem i większość z nich wydaje się wierzyć w wartość nadzoru w wykrywaniu guzów na wczesnym etapie. Zgłosili również poczucie kontroli i bezpieczeństwa związane z uczestnictwem w regularnym programie nadzoru.
Badanie dzieci pod kątem mutacji TP53
Możliwe jest testowanie dzieci i młodzieży pod kątem charakterystycznych mutacji LFS, ale pojawiły się pytania o potencjalne ryzyko, korzyści i ograniczenia tego działania, w tym brak sprawdzonych strategii nadzoru lub zapobiegania oraz obawy dotyczące stygmatyzacji i dyskryminacji.
Zalecane jest badanie osób w wieku poniżej 18 latTP53 warianty chorobotwórcze należy przeprowadzić w ramach programu, który zapewnia informacje i porady zarówno przed, jak i po teście.









.jpg)