Terapia antyretrowirusowa jest stosowana w leczeniu HIV i obejmuje połączenie leków, które blokują różne etapy cyklu replikacji wirusa. W ten sposób wirus może zostać stłumiony do niewykrywalnego poziomu, na którym może wyrządzić organizmowi niewielką szkodę.
Skuteczność skojarzonej terapii przeciwretrowirusowej została po raz pierwszy opisana przez naukowców w 1996 roku na Międzynarodowej Konferencji AIDS w Vancouver, którzy nazwali podejście HAART (wysoce aktywna terapia antyretrowirusowa).
Justin Sullivan / Getty Images News / Getty ImagesObecnie termin HAART jest rzadziej używany i został w dużej mierze wyparty w literaturze medycznej przez uproszczoną ART (terapię antyretrowirusową). Zmiana terminologii to coś więcej niż tylko semantyka; odzwierciedla zmianę celów i korzyści terapii HIV oraz odejście od tego, co historycznie sugerował HAART.
Przed HAART
Kiedy pierwsze przypadki HIV zostały zidentyfikowane w Stanach Zjednoczonych w 1982 roku, naukowcy pospiesznie szukali sposobów leczenia wirusa, który miał niewielki priorytet we współczesnej medycynie.
Minęło pięć lat, zanim pierwszy lek przeciwretrowirusowy, zwany AZT (zydowudyna), został zatwierdzony przez Amerykańską Agencję ds. Żywności i Leków (FDA) w marcu 1987 r. wyrok śmierci, może pewnego dnia zostać poddany kontroli.
Pomimo wczesnego przełomu AZT oferował jedynie niewielkie korzyści, wydłużając czas przeżycia średnio o 24 miesiące.
Szybki rozwój lekooporności spowodował, że narkotyk był coraz częściej używany, podczas gdy toksyczne działanie leku często powodowało u użytkowników ciężką anemię, problemy z wątrobą i inne nieznośne komplikacje.
Do 1988 roku trzy inne leki zostały szybko zatwierdzone - Hivid (ddC, zalcytabina), Videx (ddI, didanozyna) i Zerit (d4T, stawudyna) - i stosowane w terapiach skojarzonych w celu dalszego wydłużenia oczekiwanej długości życia. I chociaż z pewnością pomogły, okazały się jeszcze bardziej toksyczne niż AZT i wymagały skomplikowanych schematów dawkowania, często z wieloma dawkami przyjmowanymi w ciągu dnia i nocy.
Badacze szybko zaczęli zdawać sobie sprawę, że leki te - i kolejne, takie jak Viramune (newirapina) i Epivir (3TC, lamiwudyna) - nie osiągnęły trwałej kontroli, ponieważ wszystkie miały podobne mechanizmy działania i blokowały tylko jeden z siedmiu etapów cykl replikacji wirusa.
Zaproponowano, że atakując inne etapy, wirus miałby znacznie mniej możliwości replikacji i potencjalnie mógłby być w pełni kontrolowany. Ta obietnica zaczęła się urzeczywistniać w 1995 roku wraz z wprowadzeniem nowej klasy leków przeciwretrowirusowych znanych jako inhibitory proteazy (PI).
Nadejście HAART
W 1995 roku FDA zatwierdziła pierwszy inhibitor proteazy o nazwie Invirase (sakwinawir). W przeciwieństwie do innych leków przeciwretrowirusowych w tamtych czasach, które blokowały zdolność wirusa do „przejęcia” genetycznej maszynerii komórki i przekształcenia jej w fabrykę produkującą HIV, PIs zablokował zdolność wirusa do składania nowych kopii samego siebie z białek strukturalnych.
To podejście jedno-dwa okazało się punktem zwrotnym w narastającej pandemii.
Na konferencji w Vancouver w 1996 roku doniesiono, że strategiczne użycie trzech leków z każdej z dwóch klas było w stanie osiągnąć i utrzymać niewykrywalne miano wirusa, skutecznie wprowadzając chorobę w remisję.
Nowe podejście zostało szybko nazwane HAART i natychmiast wdrożone jako standard opieki. W ciągu trzech krótkich lat śmiertelność z powodu HIV w Stanach Zjednoczonych i Europie spadła o ponad 50% - był to pierwszy taki spadek od początku pandemii.
Mimo to HAART był daleki od doskonałości, a średnia długość życia, choć znacznie się poprawiła, była nadal krótsza niż w populacji ogólnej. Na przełomie XIX i XX wieku 20-latek na terapii antyretrowirusowej mógłby potencjalnie dożyć pięćdziesiątki.
W tym kontekście „wysoce skuteczny” wskazywał zarówno na ograniczenia HAART, jak i na korzyści.
Poza HAART
Do 2000 roku ograniczenia dostępnych leków przeciwretrowirusowych stały się nieuchronnie jasne. Pomimo ich zdolności do supresji wirusów, mogą stanowić ogromne wyzwanie dla użytkownika z kilku różnych powodów:
- Inhibitory proteazy w tamtym czasie wiązały się z potencjalnie ciężkimi skutkami metabolicznymi, w tym lipodystrofią (czasami zniekształcającą redystrybucję tkanki tłuszczowej), insulinoopornością i zaburzeniami rytmu serca.
- AZT, Zerit i inne leki klasyfikowane jako nukleozydowe inhibitory odwrotnej transkryptazy (NRTI) mogą powodować ciężką neuropatię obwodową i potencjalnie zagrażającą życiu kwasicę mleczanową.
- Leki w tamtych czasach były mniej „wybaczające” i podlegały szybkiemu rozwojowi lekooporności, jeśli przestrzeganie leczenia było mniej niż doskonałe. Niektóre nienukleozydowe inhibitory odwrotnej transkryptazy (NNRTI), takie jak Viramune, mogły rozwinąć oporność tylko z jedną mutacją wirusa .
- Niektóre inhibitory proteazy, takie jak Invirase, wymagały trzech kapsułek co 8 godzin - harmonogram ten dla wielu był trudny do utrzymania w dłuższej perspektywie.
Problemy te były tak problematyczne, że HAART był standardowo opóźniany, aż funkcja odpornościowa spadła poniżej pewnego progu (a mianowicie liczba CD4 poniżej 350). Uznano, że ryzyko wczesnego leczenia w tym czasie przeważało nad korzyściami.
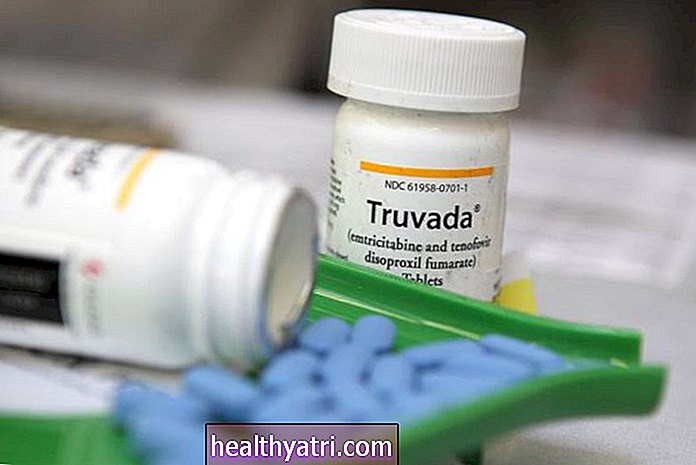
Wszystko to zmieniło się w 2001 roku wraz z wprowadzeniem Viread (fumaran tenofowiru dizoproksylu), nowego typu NRTI, który miał znacznie mniej skutków ubocznych, mógł przezwyciężyć głęboki opór i wymagał tylko jednej tabletki dziennie.
Do 2005 r., Wraz ze wzrostem oczekiwanej długości życia i spadkiem śmiertelności na całym świecie, naukowcy byli w stanie wykazać, że leczenie HIV w momencie diagnozy zapobiegało ciężkim chorobom związanym z HIV i nie związanym z HIV. choroby aż o 61%.
Ponieważ uniwersalne leczenie diagnozy stało się nowym standardem na całym świecie, społeczność medyczna zaczęła używać ART do opisania podejścia terapeutycznego, które było teraz czymś więcej niż tylko „wysoce skutecznym”.
ART Today
Główną różnicą między HAART z późnych lat 90-tych / wczesnych 2000-tych i ART obecnie jest to, że HIV naprawdę można uznać za stan przewlekły, dający się opanować. 20-latek, u którego zdiagnozowano dziś HIV, może nie tylko dożyć lat 70., ale może to zrobić dzięki lekom, które są bezpieczniejsze, trwalsze i łatwiejsze do zażywania.
Nowsze leki i ich klasy
W ostatnich latach opracowano nowsze klasy leków przeciwretrowirusowych, które atakują wirusa na różne sposoby. Niektóre zapobiegają przyczepianiu się wirusa HIV do komórek gospodarza (inhibitory wejścia / przyłączenia), podczas gdy inne blokują integrację kodującego wirusa do jądra komórki gospodarza (inhibitory integrazy).
Ponadto stworzono nowsze wersje PI, NRTI i NNRTI, które oferują lepszą farmakokinetykę (aktywność leku), mniej skutków ubocznych i lepsze profile lekooporności.
Jednym z takich przykładów jest zaktualizowana wersja preparatu Viread o nazwie alafenamid tenofowiru (TAF). Zamiast bezpośredniego dostarczania leku, TAF jest nieaktywnym „prolekiem”, który jest przekształcany przez organizm w tenofowir. Zmniejsza to dawkę z 300 mg do 25 mg z tymi samymi wynikami klinicznymi, jednocześnie zmniejszając ryzyko problemów z nerkami związanych ze stosowaniem leku Viread.
Leki złożone o ustalonej dawce
Kolejnym postępem w terapii jest opracowanie leków skojarzonych o ustalonej dawce (FDC), które mogą zapewnić pełną terapię za pomocą zaledwie jednej pigułki dziennie. Obecnie jest 13 leków typu „wszystko w jednym” zatwierdzonych przez FDA.
Preparaty w postaci pojedynczych tabletek nie tylko poprawiły wskaźniki przestrzegania zaleceń, ale wykazano, że znacznie zmniejszają ryzyko ciężkich chorób i hospitalizacji w porównaniu z terapiami przeciwretrowirusowymi złożonymi z wielu tabletek.
Nowa definicja terapii skojarzonej
Termin HAART od dawna jest synonimem terapii trójlekowej. I chociaż prawdą jest, że ART zazwyczaj składa się z trzech lub więcej leków przeciwretrowirusowych, ulepszona farmakokinetyka umożliwiła teraz leczenie HIV tylko dwoma lekami przeciwretrowirusowymi.
W 2019 roku FDA zatwierdziła pierwszą kompletną terapię dwulekową znaną jako Dovato, która łączy w sobie inhibitor integrazy nowej generacji o nazwie dolutegrawir ze starszym NRTI zwanym lamiwudyną. Kombinacja okazała się równie skuteczna jak standardowa terapia potrójna z mniejszą liczbą skutków ubocznych.
Dalszym zwrotem definicji ART na uchu było wypuszczenie w 2021 roku terapii do wstrzykiwań znanej jako Cabenuva.
Cabenuva jest pierwszymraz w miesiącuterapia umożliwiająca osiągnięcie trwałej supresji wirusa po jednym wstrzyknięciu inhibitora integrazy kabotegrawiru i jednym wstrzyknięciu nowszego NNRTI zwanego rylpiwiryną.
Postępy takie jak te na nowo definiują znaczenie ART i czym może się ostatecznie stać.
Słowo od Verywell
Chociaż cele terapii antyretrowirusowej pozostają takie same, obecnie ART tylko w niewielkim stopniu przypomina HAART z przeszłości. Bez wyjątku korzyści z leczenia znacznie przewyższają wszelkie obawy, jakie możesz mieć co do leków lub ich skutków ubocznych.
Co więcej, korzyści dotyczą również tych, którzy nie są zarażeni. Przełomowe badania opublikowane w wydaniu z 2019 rPlikLancetdoszli do wniosku, że osoby z HIV, które osiągnęły niewykrywalny wirus, mają zerową szansę na zarażenie innych.
Czynniki te dodatkowo podkreślają potrzebę wykonywania testów na obecność wirusa HIV i pokazują, dlaczego amerykańska grupa zadaniowa ds. Usług prewencyjnych zaleca jednorazowe badanie na obecność wirusa HIV u wszystkich Amerykanów w wieku od 15 do 65 lat w ramach rutynowej wizyty lekarskiej.



.jpg)