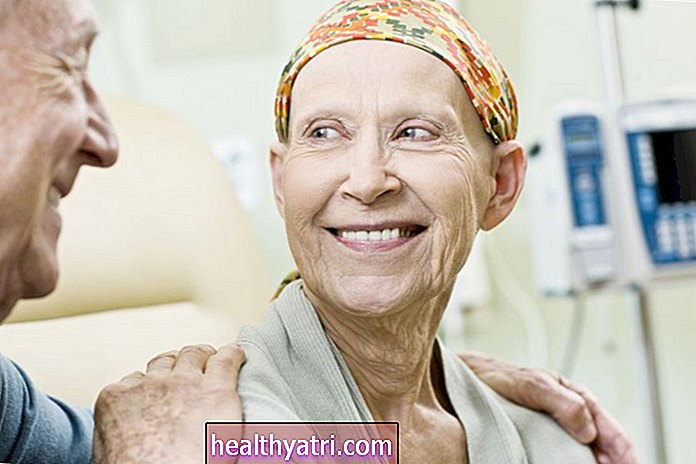
Heplisav-B jest szczepionką stosowaną w celu zapobiegania wszystkim podtypom zapalenia wątroby typu B. Została zatwierdzona przez Amerykańską Agencję ds.Żywności i Leków (FDA) 9 listopada 2017 r. Do stosowania u osób dorosłych w wieku 18 lat i starszych.
Jest to jedna z trzech szczepionek stosowanych obecnie w celu zapobiegania zakażeniu wirusem zapalenia wątroby typu B (HBV) w Stanach Zjednoczonych. Należą do nich Recombivax HB, który został zatwierdzony przez FDA w 1986 r., Oraz lider rynku Engerix-B, któremu przyznano podobne zezwolenie w 2007 r. (Istnieje również trzecia szczepionka skojarzona, znana jako Twinrix, która szczepi zarówno przeciwko wirusowemu zapaleniu wątroby typu A, jak i B. .)
Jedną z głównych zalet Heplisav-B jest to, że wymaga mniejszej liczby wstrzyknięć w krótszym okresie czasu, co może pomóc ludziom ukończyć serię, a nie zatrzymać się krótko.
Universal Images Group / Universal Images Group / Getty Images
Wstępne obawy dotyczące bezpieczeństwa
Zatwierdzenie preparatu Heplisav-B zakończyło czteroletnią walkę o wprowadzenie szczepionki na rynek. FDA wcześniej odrzuciła lek w lutym 2013 r., A później w listopadzie 2016 r. Ze względu na obawy dotyczące bezpieczeństwa dotyczące potencjalnego ryzyka ostrego zawału mięśnia sercowego (zawału serca) i niektórych chorób autoimmunologicznych.
Szczepionka została ostatecznie zatwierdzona w dużej mierze na podstawie faktu, że wymaga dwóch wstrzyknięć w odstępie miesiąca. Natomiast inne szczepionki wymagają trzech zastrzyków w odstępie jednego miesiąca, a następnie sześciu miesięcy.
Uznano to za ważne, ponieważ jedną z największych barier dla szczepień przeciw HBV jest przestrzeganie zaleceń. Badanie przeprowadzone w 2008 roku przez Departament Chorób Zakaźnych Uniwersytetu Florydy w Jacksonville wykazało, że z 707 osób kwalifikujących się do szczepienia przeciw HBV tylko 503 otrzymało dostęp do leczenia, a tylko 356 ukończyło serię trzech zastrzyków. Inne badania dały podobnie ponure wyniki.
FDA uważa, że zmniejszając lukę między wstrzyknięciami, korzyści ze szczepionki znacznie przewyższają potencjalne konsekwencje.
Skuteczność
Zatwierdzenie Heplisav-B oparto na danych z trzech badań klinicznych z udziałem ponad 14 000 dorosłych uczestników. W głównym badaniu porównano dwudawkową serię preparatu Heplisav-B z trzydawkową serią preparatu Engerix-B. Wśród 6665 uczestników biorących udział w badaniu 95% osiągnęło wysoki poziom ochrony przed Heplisav-B (mierzonym aktywnością przeciwciał) w porównaniu z 81% w przypadku Engerix-B.
W drugim badaniu z udziałem 961 osób z cukrzycą typu 2 (uważaną za grupy wysokiego ryzyka zapalenia wątroby typu B), stwierdzono, że Heplisav-B zapewnia wysoki poziom ochrony u 90% osób, którym podano szczepionkę, w porównaniu z 65% osób, którym podano Engerix. -B.
Ponadto wiadomo, że Heplisav-B zapewnia ochronę przed wszystkimi czterema głównymi serotypami, dziesięcioma genotypami (od A do J) i 40 subgenotypami.
Administracja
Heplisav-B jest podawany domięśniowo w mięsień naramienny górnej części barku. Szczepionka nie jest żywą szczepionką (zawierającą żywy, osłabiony wirus), ale zamiast tego zawiera genetycznie zmodyfikowany antygen - zasadniczo awatar wirusa - który nie powoduje choroby, ale raczej stymuluje ochronną odpowiedź immunologiczną.
Po wykonaniu pierwszego wstrzyknięcia 0,5 mililitra (ml), drugie wstrzyknięcie nastąpi w ciągu sześciu miesięcy.
Jeśli z jakiegokolwiek powodu nie możesz ukończyć serii w tym czasie, jak najszybciej porozmawiaj ze swoim lekarzem o zakończeniu serii. Jest mało prawdopodobne, że będziesz musiał ponownie uruchamiać serię.
Działania niepożądane
Chociaż niektórzy ludzie mogą doświadczyć reakcji na strzał, większość przypadków jest łagodna i ustępuje w ciągu kilku dni. Ogólnie rzecz biorąc, reakcje, jeśli w ogóle, mają tendencję do pogłębiania się po pierwszym strzale, a mniej po drugim.
Najczęstsze objawy (występujące u ponad 2% pacjentów) to:
- Obrzęk w miejscu wstrzyknięcia: 2,3%
- Zaczerwienienie w miejscu wstrzyknięcia: 4,1%
- Złe samopoczucie: 9,2%
- Ból głowy: 16,9%
- Zmęczenie: 17,4%
- Ból w miejscu wstrzyknięcia: 38,5%
Przeciwwskazania
Preparatu Heplisav-B nie należy stosować u osób, u których w wywiadzie występowały ciężkie reakcje alergiczne lub u osób, u których wcześniej wystąpiła reakcja na szczepionkę przeciw wirusowemu zapaleniu wątroby typu B lub którykolwiek z jej składników, w tym drożdżaki. Ponowna ekspozycja może spowodować potencjalnie zagrażającą życiu, ogólnoustrojową reakcję alergiczną znaną jako anafilaksja.
Jak dotąd nie przeprowadzono badań na ludziach dotyczących wpływu Heplisav-B podczas ciąży lub karmienia piersią. Jednak badanie na zwierzętach nie wykazało żadnych działań niepożądanych u ciężarnych szczurów laboratoryjnych ani ich potomstwa po podaniu dawki 0,3 ml preparatu Heplisav-B.
Kto powinien się zaszczepić
Wirusowe zapalenie wątroby typu B to wirusowa choroba wątroby, która może stać się przewlekła i prowadzić do marskości, raka wątroby i śmierci.
Według raportu amerykańskiej grupy zadaniowej ds. Usług prewencyjnych (USPSTF), od 700 000 do 2,2. Uważa się, że w Stanach Zjednoczonych milion ludzi jest zarażonych HBV. Wskaźniki infekcji są najwyższe wśród osób dorosłych w wieku od 30 do 49 lat, z których większość zaraża się poprzez seks bez zabezpieczenia lub używanie wspólnych igieł.
Nie ma lekarstwa na wirusowe zapalenie wątroby typu B, ale skuteczne szczepienie może zapobiec chorobie. Z tego powodu Komitet Doradczy ds. Praktyk Szczepień (ACIP) i obecnie zaleca, aby wszystkie dzieci otrzymały pierwszą dawkę szczepionki przeciw HBV zaraz po urodzeniu i ukończyły serię w okresie od 6 do 18 miesięcy. Należy również zaszczepić starsze dzieci i młodzież, które nie otrzymały szczepionki przeciw HBV.
Centers for Disease Control and Prevention zaleca ponadto szczepienie wszystkich dorosłych osób z wysokim ryzykiem zakażenia HBV. Obejmują one:
- Osoby, które mieszkają lub uprawiają seks z osobą chorą na wirusowe zapalenie wątroby typu B.
- Osoby aktywne seksualnie, które nie pozostają w długotrwałym, wzajemnie monogamicznym związku
- Osoby poszukujące badań lub leczenia zakażenia przenoszonego drogą płciową
- Mężczyźni uprawiający seks z mężczyznami
- Osoby żyjące z HIV
- Osoby, które mają wspólne igły, strzykawki lub inne akcesoria związane z narkotykami
- Pracownicy służby zdrowia i inne osoby narażone na kontakt z krwią
- Osoby ze schyłkową niewydolnością nerek
- Osoby z przewlekłą chorobą wątroby
- Osoby z cukrzycą w wieku poniżej 60 lat rozpoczęły leczenie tak szybko, jak to możliwe po postawieniu diagnozy
- Osoby podróżujące z zagranicy do regionów o umiarkowanych do wysokich wskaźnikach wirusowego zapalenia wątroby typu B
- Osoby, które imigrowały z krajów o umiarkowanym lub wysokim wskaźniku zapalenia wątroby typu B lub dzieci urodzone przez rodziców, którzy wyemigrowali z tych krajów przed urodzeniem
- Każdy, kto uważa się za zagrożonego
USPSTF nie zaleca obecnie szczepień przeciw HBV dla ogólnej populacji dorosłych, ponieważ nie wykazano, że praktyka ta zmniejsza ryzyko chorób wątroby lub zgonu.
Analiza obaw dotyczących bezpieczeństwa
Pomimo w dużej mierze pozytywnego odbioru przez urzędników ds. Zdrowia publicznego, szczepionka nadal dręczy obawy dotyczące bezpieczeństwa, biorąc pod uwagę jej wczesne odrzucenie przez FDA.
FDA początkowo odrzuciła szczepionkę w 2013 r. W oparciu o jeden z jej składników, znany jako CpG 1018. Jest to związek używany do wzmacniania zdolności wywoływania odporności przez szczepionkę i ten, który umożliwia serię dwóch zastrzyków.
Zgodnie z odpowiedzią FDA, uważa się, że CpG 1018 może wywoływać pewne zaburzenia autoimmunologiczne, w tym chorobę tarczycy. Podczas gdy wczesne badania nie wykazały statystycznej różnicy między Heplisav-B i Engerix-B, wniosek został odrzucony tylko dlatego, że rozmiar badania w tamtym czasie uznano za zbyt mały.
Do czasu ponownego podania szczepionki podano 14 238 osobom, przy czym odnotowano tylko dwa przypadki zapalenia tarczycy Hashimoto (forma choroby tarczycy) i jeden przypadek bielactwa nabytego.
Później, w 2016 roku, szczepionka została również odrzucona, gdy w jednym badaniu odnotowano większą niż oczekiwano liczbę zdarzeń sercowych, w tym zawały serca. W tym przypadku FDA zażądała dodatkowych informacji dotyczących wszelkich niezwiązanych z nimi czynników, które mogłyby pomóc w lepszym wyjaśnieniu wyników.
Po zapoznaniu się z dodatkowymi danymi, FDA udzieliła zgody. Końcowe wyniki badań wykazały 0,1% ryzyko zawału serca u osób, którym podawano Heplisav-B w porównaniu z 0,2%, którym podawano Engerix-B.















.jpg)