Pool / Pool / Getty Images
Kluczowe wnioski
- FDA przyznała zezwolenie na stosowanie w nagłych przypadkach szczepionce COVID-19 opracowanej przez Pfizer i BioNTech.
- Wiadomość pojawiła się dzień po tym, jak komitet doradczy FDA zalecił agencji autoryzację szczepionki
- Dane przeanalizowane przez komisję wykazały skuteczność szczepionki w 95%.
- Dystrybucja szczepionek może nastąpić w ciągu 24 godzin od uzyskania pozwolenia.
Food and Drug Administration (FDA) przyznała zezwolenie na stosowanie w nagłych wypadkach pierwszej szczepionki COVID-19 w piątek wieczorem. Szczepionka, opracowana przez Pfizer Inc. i niemiecką firmę BioNTech, wkrótce rozpocznie dystrybucję.
Wiadomość jest następstwem długo oczekiwanego przesłuchania publicznego w czwartek, podczas którego panel doradczy FDA głosował 17-4 za zezwoleniem na szczepionkę Pfizera, przy jednym wstrzymującym się.
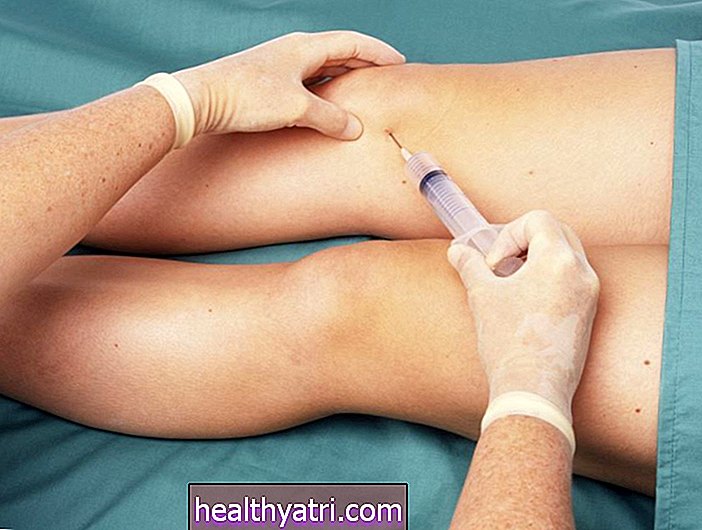
Firma Pfizer przedstawiła dane z badań klinicznych z udziałem 43 000 dorosłych uczestników. Na początku tego tygodnia FDA udostępniła niektóre z tych danych, w tym fakt, że 95% osób biorących udział w badaniu klinicznym, które otrzymały szczepionkę, nie rozwinęło COVID -19. Efekty uboczne były niewielkie, w tym dreszcze, łagodny ból i zaczerwienienie w miejscu wstrzyknięcia.
Zezwolenie na użycie w nagłych wypadkach (EUA) dotyczy osób w wieku 16 lat i starszych. Firma Pfizer prowadzi również badania kliniczne dotyczące bezpieczeństwa i skuteczności szczepionki u dzieci w wieku 12 lat i oczekuje się, że doda również badania dla młodszych dzieci.
Dane dotyczące bezpieczeństwa i skuteczności pochodzące z większej liczby populacji, które są nadal potrzebne
Panel doradczy FDA, zwany Komitetem Doradczym ds. Szczepionek i Pokrewnych Produktów Biologicznych (VRBPAC), zaleca firmie Pfizer podjęcie dodatkowych środków, aby upewnić się, że szczepionka jest bezpieczna i skuteczna dla większej liczby populacji. Panel zaleca włączenie większej liczby osób kolorowych do trwających badań klinicznych. Osoby kolorowe częściej niż biali zarażają się COVID-19 i umierają z powodu wirusa.
Panel omówił również dwa zgłoszone przypadki reakcji alergicznych u osób, które otrzymały szczepionkę w Wielkiej Brytanii w tym tygodniu, gdzie została ona już zatwierdzona. Dr Paul Offit, dyrektor Centrum Edukacji Szczepionkowej w Szpitalu Dziecięcym w Filadelfii, zapytał prezenterów firmy Pfizer o reakcje alergiczne, obawiając się, że osoby z ciężkimi alergiami mogą zrezygnować z przyjmowania szczepionki. Offit zalecił również przeprowadzenie badań szczepionki u osób z powszechnymi alergiami.
Wielka Brytania zaleca, aby osoby z historią anafilaksji związanej z lekami lub żywnością nie otrzymywały szczepionki. Stany Zjednoczone mogą dodać podobne ostrzeżenie wraz z uzyskaniem zezwolenia. Pracownicy FDA na spotkaniu powiedzieli panelowi, że już pracują nad pisemną dokumentacją dla konsumentów dotyczącą bezpieczeństwa i skuteczności szczepionki.
Co to oznacza dla Ciebie
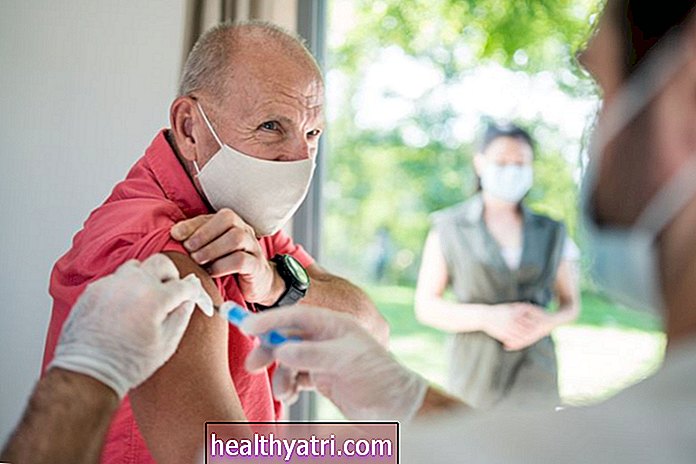
Na podstawie zalecenia komitetu doradczego dotyczącego autoryzacji szczepionki COVID-19 firmy Pfizer, Agencja ds.Żywności i Leków mogła zatwierdzić jej użycie w ciągu kilku dni. Dystrybucja mogłaby się rozpocząć wkrótce potem.Oczekuje się, że pierwsze dawki szczepionki zostaną podane pracownikom służby zdrowia i mieszkańcom domów opieki.
Po decyzji VRBPAC komisarz FDA, dr Stephen M. Hahn, wydał oświadczenie:
„Zwykle proces przeglądu szczepionek przebadanych na dziesiątkach tysięcy ludzi trwa miesiące. Mimo że proces został przyspieszony w związku z przeglądem niniejszego EUA, eksperci FDA przejrzeli tysiące stron informacji technicznych [w tym] danych z badań klinicznych, danych nieklinicznych dotyczących rozwoju szczepionki w laboratorium, i dane produkcyjne dotyczące sposobu wytwarzania szczepionki ”.
Hahn, prawdopodobnie starając się rozwiać obawy konsumentów, dodał: „W tym pilnym czasie pracownicy FDA czują się zobowiązani do jak najszybszego przejścia przez proces przeglądu. Jednak wiedzą, że muszą wypełniać swój mandat, aby chronić zdrowie publiczne i zapewnić, że każda autoryzowana szczepionka spełnia nasze rygorystyczne standardy bezpieczeństwa i skuteczności, których Amerykanie przyzwyczaili się oczekiwać ”.
Prezydent elekt Joe Biden wydał również oświadczenie po głosowaniu w komisji, w którym stwierdził, że „rzetelność nauki doprowadziła nas do tego punktu”.
FDA twierdzi, że dystrybucja szczepionek może nastąpić w ciągu 24 godzin od autoryzacji.
Komitet doradczy FDA dokona przeglądu drugiej szczepionki COVID-19, wyprodukowanej przez Moderna, w czwartek 17 grudnia.






-for-osteoarthritis.jpg)





.jpg)