Margaret Johnson / EyeEm / Getty Images
Kluczowe wnioski
- Firma Johnson & Johnson wstrzymała badania kliniczne swoich szczepionek COVID-19 w wyniku nieujawnionej choroby u jednego z uczestników.
- Poważne zdarzenia niepożądane (SAE) nie są rzadkie. Oczekuje się ich podczas prób szczepionek.
- Johnson & Johnson jest drugą firmą, która wstrzymała badania szczepionek podczas Fazy 3. AstraZeneca wstrzymała badania w zeszłym miesiącu.
AKTUALIZACJA: 23 października firma Johnson & Johnson ogłosiła wznowienie badania klinicznego III fazy w USA
Firma Johnson & Johnson wstrzymała badania kliniczne swoich szczepionek COVID-19 12 października w wyniku „niewyjaśnionej choroby” u jednego z uczestników.
„Zgodnie z naszymi wytycznymi choroba uczestnika jest analizowana i oceniana przez niezależną Radę ds. Monitorowania Bezpieczeństwa Danych (DSMB) ENSEMBLE, a także przez naszych wewnętrznych lekarzy ds. Klinicznych i bezpieczeństwa” - podała firma w oświadczeniu. „Zdarzenia niepożądane - choroby, wypadki itp. - nawet te poważne, są oczekiwaną częścią każdego badania klinicznego, zwłaszcza dużych badań”.
Kontynuowali: „Opierając się na naszym silnym zaangażowaniu w bezpieczeństwo, wszystkie badania kliniczne przeprowadzone przez Janssen Pharmaceutical Companies of Johnson & Johnson miały z góry określone wytyczne. Dzięki temu nasze badania mogą zostać wstrzymane w przypadku zgłoszenia nieoczekiwanego poważnego zdarzenia niepożądanego (SAE), które może być związane ze szczepionką lub badanym lekiem, dzięki czemu przed podjęciem decyzji o wznowieniu badania można dokładnie przejrzeć wszystkie informacje medyczne. ”
Janssen Pharmaceutical Companies firmy Johnson & Johnson opracowuje szczepionkę. Chociaż firma nie powiedziała, na czym polega choroba, zauważyła, że „muszą szanować prywatność tego uczestnika”. Janssen powiedział również w oświadczeniu, że jest zdecydowany dowiedzieć się więcej o chorobie uczestnika, zanim podzieli się dodatkowymi szczegółami.
„SAE nie są rzadkością w badaniach klinicznych, a można rozsądnie oczekiwać, że liczba SAE wzrośnie w badaniach z udziałem dużej liczby uczestników” - czytamy w oświadczeniu. „Ponadto, ponieważ wiele badań jest kontrolowanych placebo, nie zawsze jest to od razu widoczne czy uczestnik otrzymał badany lek, czy placebo. ”
Co oznacza pauza?
Przerwa niekoniecznie jest powodem do niepokoju - mówi dr Julian Rosenberg, zastępca dyrektora Centrum Edukacji i Szkolenia Biofarmaceutycznego. W rzeczywistości można się tego spodziewać.
„Obecnie tempo opracowywania szczepionek przeciwko SARS-CoV-2 przebiega w przyspieszonym tempie, przy dodatkowej presji intensywnej globalnej uwagi” - mówi Verywell. „Przerwy w badaniach klinicznych po prostu pokazują, że nasz rygorystyczny system regulacyjny działa”.
Soma Mandal, lekarz internista z dyplomem zarządu Summit Medical Group w Berkeley Heights w stanie New Jersey, zgadza się z tym.
„Jest to rutynowe i nie powinno budzić niepokoju, ponieważ jest częścią procesu w randomizowanej kontrolowanej próbie” - mówi Verywell. „Istnieją standardowe procesy przeglądu, które są uruchamiane w przypadku wystąpienia potencjalnie niewyjaśnionej choroby. Wskazuje to, że badacze są zaangażowani w bezpieczeństwo uczestników, a badanie jest prowadzone zgodnie z najwyższymi standardami”.
Johnson & Johnson szybko wskazał w swoim oświadczeniu, że istnieje również różnica między wstrzymaniem badania a wstrzymaniem regulacyjnym.
„Przerwa w badaniu, w której rekrutacja lub dawkowanie jest wstrzymywane przez sponsora badania, jest standardowym elementem protokołu badania klinicznego” - powiedział Johnson & Johnson w komunikacie prasowym. „Zawieszenie badania klinicznego jest wymagane przez organ regulacyjny ds. Zdrowia, taki jak amerykańska Agencja ds. Żywności i Leków. Zgodnie z naszymi zobowiązaniami dotyczącymi przejrzystości, proaktywnie ujawniamy wszelkie regulacyjne wstrzymanie kluczowego badania klinicznego”.
Johnson & Johnson jest drugą firmą, która wstrzymała badania szczepionek podczas fazy 3. Badanie AstraZenca zostało wstrzymane w zeszłym miesiącu w wyniku wystąpienia u pacjenta zapalenia rdzenia kręgowego zwanego poprzecznym zapaleniem rdzenia kręgowego. Chociaż AstraZeneca wznowiła badania 12 września w Wielkiej Brytanii, badania kliniczne firmy w innych krajach są nadal wstrzymane.
„Nauka rzadko przebiega doskonale” - mówi Rosenberg. „Gdyby tak było, nie musielibyśmy przeprowadzać eksperymentów”.
Co to jest badanie kliniczne?
W tym momencie możesz się zastanawiać, jak działają próby szczepionek. Według Center for Virology and Vaccine Research (CVVR) „badanie kliniczne to badanie prowadzone z udziałem ludzi. Każdy lek, który jest licencjonowany i zatwierdzony do użytku przez FDA, zaczyna się od badań klinicznych ”.
Środki bezpieczeństwa podczas badań klinicznych obejmują regularne kontrole w celu oceny ważnych parametrów życiowych, w tym ciśnienia krwi, temperatury i, w niektórych przypadkach, badania krwi.
„Zazwyczaj zdarzenia niepożądane nie są rzadkie i często nie są ze sobą powiązane, ale naukowcy muszą dołożyć wszelkich starań, aby upewnić się, że nie ma nic związanego z samą szczepionką” - mówi Mandal. „Niezależny komitet analizuje dane, a następnie określa, czy szczepionka spowodowała niepożądane zdarzenie. Jeśli zostanie ustalone, że nie ma korelacji, próba może być kontynuowana.
Firma Johnson & Johnson rozpoczęła badania kliniczne w lipcu.
Co to oznacza dla Ciebie
Przerwa w badaniach klinicznych nie oznacza, że cały postęp w kierunku szczepionki COVID-19 został zatrzymany. Kilka firm farmaceutycznych nadal podejmuje kroki naprzód, zapewniając, że szczepionka COVID-19 zostanie ostatecznie zatwierdzona, wyprodukowana i publicznie dostępna.
Jakie są fazy opracowywania szczepionki?
Jak można się domyślić, proces opracowywania szczepionki składa się z wielu faz - dokładnie sześciu. Według Centers for Disease Control and Prevention (CDC), Faza 1 obejmuje małe grupy osób otrzymujących próbną szczepionkę. W fazie 2 badanie kliniczne rozszerza się i szczepionkę otrzymują osoby, które mają cechy (takie jak wiek i stan zdrowia fizycznego) podobne do tych, które są objęte szczepionką. Podczas fazy 3 „szczepionka jest podawana tysiącom ludzi i testowana pod kątem skuteczności i bezpieczeństwa”, zauważa CDC.
Stamtąd Fazy 4, 5 i 6 obejmują przegląd regulacyjny i zatwierdzenie, produkcję i kontrolę jakości, co obejmuje ciągłe monitorowanie zaszczepionych osób w celu zapewnienia stałego bezpieczeństwa.
Objawy i skutki uboczne związane ze szczepionką są śledzone w systemie Vaccine Adverse Event Reporting System (VAERS), krajowym programie nadzoru bezpieczeństwa szczepionek współsponsorowanym przez Food and Drug Administration (FDA) i CDC.
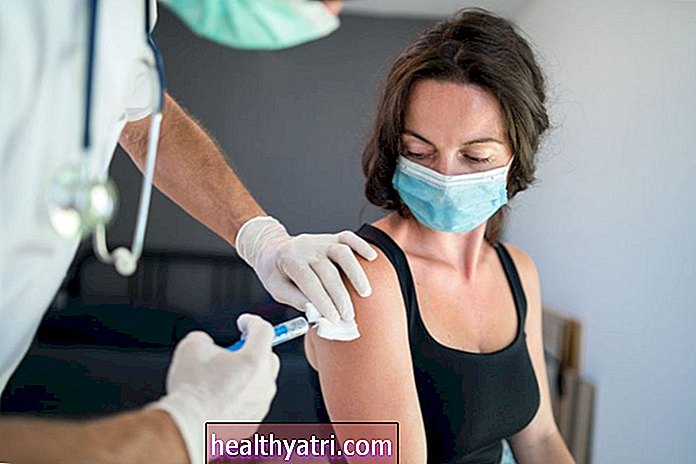
Aż do szczepionkimazostało zatwierdzone, zaleca się dalsze stosowanie protokołów bezpieczeństwa, w tym noszenie maski, regularne mycie rąk i utrzymywanie bezpiecznego dystansu społecznego.
Szczepionki COVID-19: bądź na bieżąco z dostępnymi szczepionkami, kto może je otrzymać i jak są bezpieczne.















-side-effects.jpg)